Après les bénéfices obtenus dans le mélanome métastatique grâce à l’ipilumimab, l’immunothérapie est à l’étude toujours dans les mélanomes mais, également, dans les CBNPC, avec des premiers résultats prometteurs.
L’immunothérapie est donc en plein essor, avec plusieurs molécules en développement.
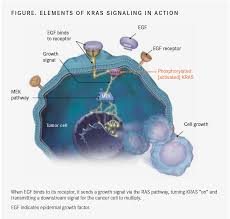
Après l’ipilumimab, qui bloque le CTLA-4(antigène du lymphocyte T Cytotoxique 4), exprimé à la surface des lymphocytes T, apparaissent de nouveaux anticorps monoclonaux contre la molécule de costimulation PD-1(Programmed cell Death-1) exprimé à la surface des lymphocytes T, et son ligand, le PDL-1, exprimé par les cellules tumorales.
Quand le récepteur et son ligand sont liés, une sorte de bouclier se forme, “rendant invisible” la cellule cancéreuse au système immunitaire du patient. Les anti-PD-1 et les anti-PDL-1 bloquent cette liaison et permettent au système immunitaire de reconnaître et de réagir contre la cellule cancéreuse. Il existe, également, une autre protéine, PD-2, avec un autre ligand.
Contrairement à l’ipilimumab, qui agit uniquement sur les lymphocytes T, les anti-PD-1 et anti-PDL-1 agissent, eux, non seulement sur les lymphocytes T mais aussi B et NK.
Plusieurs molécules anti-PD-1 ont un développement avancé: nivolumab, lambrolizumab. Parmi les anti-PDL-1 sont en développement le MPDL 3280A et le BMS 936559
►Dans le mélanome métastatique
NIVOLUMAB, anti PD-1
Après les résultats encourageants présentés au congrès annuel de l'ASCO l'année dernière, de nouvelles données à plus long terme présentés à l'ASCO 2013 confirment que l'anticorps monoclonal anti PD-1, le nivolumab de BMS induit des taux de réponse jusque-là inégalés chez les patients atteints de mélanome métastatique.
Dans cet essai de phase 1, 33 des 107 (31 %) patients en échec thérapeutique et traités par le nivolumab pour un mélanome métastatique ont eu une réponse objective (rétrécissement de la tumeur d'au moins un tiers). Les réponses ont été observées pour les 5 doses testées.
Dans les deux cas, ces taux sont supérieurs aux taux de 5 à 10% observés avec les autres immunothérapies utilisées dans le mélanome métastatique.
Les taux de survie globale étaient de 44% à 2 ans et de 40 % à 3 ans. Cependant, les taux de survie ont été calculés sur un faible nombre de patients, et il est trop tôt pour connaître les implications réelles de ces données. La dose de 3 mg/kg va, de fait, être évaluée dans un essai de phase III chez des patients atteints de mélanome métastatique.
82 % des patients qui ont reçu le nivolumab ont eu des effets secondaires mais les effets secondaires de grade III/IV sont survenus chez seulement 21 % d'entre eux. Les effets secondaires les plus fréquents étaient la lymphopénie (3%), la fatigue, et un taux de lipase augmenté (2%).
Les effets secondaires de grade III/IV étaient la diarrhée (2%), les problèmes endocriniens (2%) et les hépatites (1%). Aucune pneumopathie sévère et aucun décès liés au médicament n'ont été observés dans la cohorte. Les patients enrôlés dans l'étude étaient fortement prétraités : 63% avaient reçu au moins deux thérapies auparavant et un quart au moins 3 traitements.
LAMBROLIZUMAB, anti-PD-1
Suivant les traces de résultats positifs du nivolumab, un autre anticorps anti-PD1, le lambrolizumab (anciennement MK-3475), de MERCK montre aussi une activité prometteuse dans le mélanome. L’étude de phase IAt the annual meeting of the American Society of Clinical Oncology, Antoni Ribas, MD, PhD, of the Jonsson Comprehensive Cancer Center at the University of California, Los Angeles, presented data from a large, 1,000-plus patient phase I trial that also included other cancer types., dirigée par le service de dermatologie de l’IGR,Of the 135 metastatic melanoma patients treated with lambrolizumab at different doses, 38% had their tumors shrink in volume by at least 30%. portait sur des patients préalablement traités par l'ipilimumab. L'essai clinique a été mené avec 135 patients souffrant d'un mélanome avancé entre décembre 2011 et septembre 2012, montrant une réduction moyenne de 38 % de la tumeur. La réduction la plus forte a été de 52 %. Le traitement semble avoir un faible taux de toxicité et un spectre différent de toxicité par rapport à ceux observés dans les essais ipilimumab, mais des essais plus importants sont nécessaires pour confirmer cette observation. Of the patients treated with at least one dose of the antibody, 79% had a drug-related toxicity.The most common high-grade toxicities were skin rash in three patients, increased liver enzymes in two patients, renal failure in two patients, and fatigue in two patients. Les toxicités les plus courantes ont été des éruptions cutanées chez trois patients, augmentation des enzymes du foie chez deux patients, l'insuffisance rénale chez deux patients, et la fatigue chez deux patients. Patients who were previously treated with immunotherapies, including ipiliumab, did not have higher rates of adverse events. Les patients ayant déjà été traités avec des immunothérapies, y compris ipilimumab, n'ont pas des taux plus élevés d'événements indésirables. Une étude de phase III va débuter.
NIVOLUMAB + IPILIMUMAB
Une étude de phase III débute avec un schéma séquentiel ou concomitant.
►Dans le CBNPC avancé (stade IIIB ou IV)
NIVOLUMAB, anti PD-1
Une étude de phase I chez 129 patients lourdement prétraités (54% avec 3 ou + lignes de chimiothérapie) ont reçu 10mg/kg IV de nivolumab toutes les 2 semaines pendant au moins 12 cycles.
La médiane de survie est de 9.2 mois dans les cancers épidermoides et de 10.1 mois dans les CNBPC non épidermoides avec des taux de survie à un an de 39% et 43% respectivement.
Des effets secondaires essentiellement cutanés et gastro-intestinaux et peu d’événements grade III/IV observés (fatigue, pneumonie, élévation des transaminases).
MPDL 3280A, anti-PDL-1
Cet anticorps monoclonal bloquant le ligand PDL-1 a été testé en phase I dans les CBNPC, localement avancés ou métastatiques.
La protéine PDL-1 est exprimée dans 50% des CBNPC.
Le MPDL 3280A a été utilisé en monothérapie, chez 41 patients, aux doses de 10 et 20mg/kg IV toutes les 3 semaines. Le taux de réponse globale était de 22% avec 33% pour les formes épidermoides et 19% pour les non épidermoides.
Un statut PDL-1 positif augmentait le taux de réponses jusqu’à 100% pour les épidermoides. Il n’y a eu aucun cas d’atteinte pulmonaire, mais des cas de péricardite, d'asthénie, de diarrhée, de troubles métaboliques (hyponatrémie, hyperglycémie).
La toxicité de ces molécules est particulière avec des signes d’auto-immunité, des rashs, des diarrhées, des anomalies thyroïdiennes, des atteintes pulmonaires interstitielles potentiellement graves, nécessitant une corticothérapie à forte dose et d’instauration rapide. L’appréciation de la réponse est aussi une question délicate car des cas d’aggravation des images radiologiques, durant les premières semaines de traitement, ont été rapportés, avant qu’une réponse n’apparaisse après 6 à 12 semaines. Il est parfois difficile de trancher et il faut savoir si l’état du patient est stable, poursuivre le traitement ou réaliser des prélèvements.
D’après les critères RECIST pour les tumeurs solides, une augmentation précoce du volume tumoral ou la survenue de nouvelles lésions sont classifiées comme «progressive disease», ce qui équivaut à un échec thérapeutique dans les études cliniques. Compte tenu du mécanisme d’action de principes actifs comme l’ipilimumab ou les anti-PD-1, qui renforcent la réaction immunitaire, de nouveaux critères radiologiques de réponse tumorale irRC (immunerelated Response Criteria) ont été définis car avec ces molécules, la régression peut être précédée d’une augmentation du volume tumoral. L’augmentation initiale du volume tumoral pourrait être attribuable à une réaction inflammatoire locale suite au recrutement des cellules T activées et à une infiltration de la tumeur par des cellules T. Par ailleurs, une réponse est également possible si de nouvelles lésions sont apparemment présentes.
Il sera peut être utile de rechercher, par immunohistochimie, le niveau d’expression de PD1 et PDL-1 et de sélectionner les patients en fonction du statut. Des résultats préliminaires ont montré que chez les 5 patients dont la tumeur était PDL-1 positive, il y a eu 4 réponses objectives et 1 stabilisation de la maladie ; il y avait, a contrario, 4 réponses sur 28 patients PDL-1 négative.
Le développement de ces molécules d’immunothérapie est donc à suivre de près.