| Les données biologiques récentes ont remis en cause la notion de prolifération androgéno-indépendante lors de la résistance à la castration avec la démonstration maintenant bien étayée que l’axe androgène/récepteur aux androgènes (RA) continuait à jouer un rôle majeur dans la prolifération tumorale à ce stade.
Les résultats en clinique de l’acétate d’abiraterone ont clairement validé le concept.
►Une étude clinique monocentrique a été réalisée au MD Anderson (Efstathiou E, Titus M, Tsavachidou D et al.) auprès de 57 patients présentant un CPRC avec métastases osseuses dont 40 avaient eu une biopsie osseuse iliaque, tous traités par l’acétate d’abiraterone et prednisone. Cette étude était ouverte, observationnelle et translationnelle avec une étude en immunohistochimie de l’expression du RA et du CYP17 (l’enzyme cible de l’acétate d’abiraterone), du nombre de copies de RA par PCR et de la présence de gène de fusion TMPRSS2-ERG par FISH quand cela était techniquement possible. Une mesure de la concentration de la testostérone et de la dihydrotestostérone (DHT) était réalisée dans le sang et la moelle osseuse, le deuxième objectif étant de mesurer les taux d’androgènes circulants avant et sous traitement par l’acétate d’abiraterone et de les corréler à la réponse.
►L’analyse des données préliminaires d’une large cohorte de 381 patients français ayant bénéficié d’une ATU avait également retrouvé deux populations de patients répondeurs et non répondeurs aux pronostics très différents (Azria D, ASCO GU). ►Une analyse récente à partir de l’étude COU-AA-301 vient de montrer l’importance des taux sanguins initiaux élevés des androgènes (testostérone, DHEA, androstenedione) comme facteur prédictif de survie (Ryan C, AACR 2012). |
►Réarrangement ERG et résultats cliniques chez les patients chimio-naïfs traités par
l’acétate d’abiraterone dans l’une étude COU-AA-302, dans le cancer de la prostate
métastatique résistant à la castration.
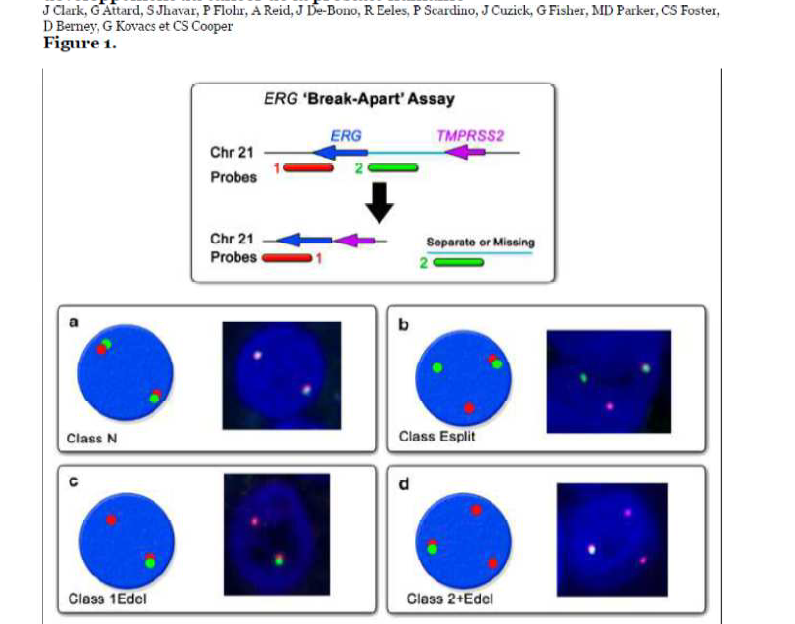
Rappel sur la fusion TMPRSS2-ERG
La translocation la plus fréquente dans le cancer de la prostate est une fusion du gène modelé par les androgènes TMPRSS2 avec un gène de la famille des facteurs
de transcription ETS. ETS codent pour des facteurs de transcription intervenant dans les voies de signalisation régulant la croissance cellulaire, la différenciation, la réponse au stress et la tumorigénèse. Le gène TMPRSS2 code pour la sérine protéase transmembranaire 2 qui est une protéine multimère à domaine sérine-protéase contrôlée par les androgènes.
La mise en évidence récente de gènes de fusion TMPRSS2—ETS dans plus de la moitié des cancers de la prostate a été une véritable révolution dans la connaissance
biologique de ces tumeurs. De tous les facteurs de transcription ETS (ERG, ETV1, ETV4), le gène ERG est le partenaire de fusion le plus fréquent du TMPRSS2, plus rarement le gène ETV1.
Les gènes spécifiques de la prostate TMPRSS2 et ERG à régulation androgénique sont distants d’environ trois mégabases sur le chromosome 21. La fusion de ces gènes survient avec ou sans délétion des régions du DNA situées entre ces deux gènes. Une alternative est l’insertion de ce fragment de DNA dans un autre endroit du génome, situé en-dehors du chromosome 21.
Un test moléculaire urinaire permet de détecter et d’évaluer quantitativement le score T2:ERG.
L’expression de la fusion TMPRSS2:ERG dans les cellules prostatiques cancéreuses est un facteur pronostic important de la progression tumorale. Les patients ayant la protéine de fusion ont un taux de récidive plus élevé que ceux n’ayant pas la protéine. L’expression de la fusion TMPRSS2:ERG est un indicateur très fiable de la récidive.
Le score T2:ERG dans l’urine était corrélé avec le score de Gleason, le nombre de carottes positives et le pourcentage d’envahissement des carottes des biopsies. Le score T2:ERG paraît également corrélé avec le degré d’agressivité de la tumeur. Ce test pourrait donc être un complément idéal du dosage du taux de PSA.
L’analyse du statut ERG donne lieu à plusieurs classes.
Classe N : aucun réarrangement ERG ne s’est produit.
Classe Edel : réarrangement ERG conséquent à la perte d’une délétion
Edel 2+ : Délétion interstitielle avec duplication des séquences de fusion
Edel 1 : Délétion interstitielle
Classe Esplit : réarrangement sans délétion interstitielleNearly half of the peripheral tumours (43.3%) derived from RP samples were ERG rearrangement positive, whereas all 30 corresponding transitional tumours displayed a normal ERG locus by FISH (Guo et al., 2009).
A l’inverse du PSA, qui est spécifique du tissu prostatique, mais pas du carcinome prostatique, cette translocation est donc nettement plus spécifique que le PSA. La spécificité et la sensibilité peuvent encore être augmentées en combinant la détermination de la fusion TMPRSS2ERG, le screening du PSA et la mesure d’autres biomarqueurs.
Les hommes atteints d’un cancer de la prostate TMPRSS2ERG androgène dépendant profitent probablement dans une plus grande mesure d’un traitement antiandrogénique.
Rationnel de l’étude
En cas de résistance à la castration, les gènes de fusion ont pris une place au sein des facteurs pronostiques dans le cancer de la prostate.
L’augmentation de l’expression de la protéine ERG, suite aux réarrangements ERG, sont associés à un mauvais pronostic dans le CPRC.
Et cette augmentation est susceptible de modifier la réponse au traitement par l’acétate d’abiraterone.
Résultats
|
Etude |
ERG non Réarrangé |
ERG Réarrangé |
Esplit |
Edel1 |
Edel 2+ |
|
COU-AA-02 n=342 |
224 65.5%) | 118 (34.5%) | 6 (1.8%) | 62 (18.1%) | 50 (14.6%) |
Dans le bras acétate d’abiraterone, il y a une tendance en faveur d’une association entre le statut ERG et la survie sans progression.
Aucun impact n’a été démontré sur la survie globale.
L’acétate d’abiraterone augmente la médiane de survie sans progression de 5.4 à 22 mois en cas de réarrangement Edel 2+ (HR=0.3 ; IC 95% :0.14-0.67) et seulement de 8 à 16 mois en cas d’ERG non réarrangé.
Aucune association entre le statut ERG et la survie sans progression pour le bras prednisolone seule.
Le statut ERG pourrait être un facteur prédictif de réponse avec une tendance à l’amélioration de la survie sans progression clinique et biologique chez les patients ayant un réarrangement ERG de type Edel 2+ et traités par l’acétate d’abiraterone.
►Un nouvel essai clinique, financé par l'Institut national du cancer subvention N01-CM-2011-00071C, subvention du ministère de la Défense PC080189 États-Unis, et la Prostate Cancer Foundation, va être mis en place chez les patients résistant à la castration.
The target of this phase II trial of patients with castration-resistant metastatic prostate cancer is a genomic rearrangement that causes the genes TMPRSS2 and ERG to fuse together. Study DetailsStudy participants will undergo a biopsy to determine whether their tumor expresses the gene fusion, which occurs in about half of all prostate cancers. Les participants à cette étude de phase II seront soumis à une biopsie afin de déterminer si la tumeur exprime le gène de fusion.All participants will receive the standard hormone-based therapy abiraterone (Zytiga). Tous les participants recevront l’acétate d’abiraterone associé à la prédnisone. La moitié des participants se verront en plus attribuer le Veliparib, inhibiteur de PARP et connu pour agir sur la fusion des gènes TMPRSS2 et ERG.
Cette étude a pour objectif de déterminer si l’association à l’acétate d’abiraterone donnera de meilleurs résultats chez les patients exprimant le gène de fusion.ABT-888 is a PARP inhibitor that is known to directly interact with the TMPRSS2:ERG gene fusion, leading to cancer growth and progression.
Actuellement, au stade métastatique résistant à la castration, la prise en charge des patients connait une vraie révolution avec l’apparition de traitements différents : l’acétate d’abiraterone, l’enzalutamide, le cabazitaxel et le sipuleucel T.
Plusieurs possibilités seront donc possibles pour les patients résistant à la castration. Concernant le Zytiga®, une expression tumorale de CYP17 ≥ 10%, des concentrations plus élevées en testostérone au niveau sanguin et médullaire et un réarrangement Edel 2+ pourraient être corrélés avec la réponse thérapeutique.